Deux articles sur ce sujet – voici le premier et le plus amusant.
Les injections à venir: le Japon approuve de nouveaux vaccins Covid sur base des données relatives aux anticorps
30 nov. 2023
De l’ARNm maison
Après s’être fait injecter pendant des années de l’ARNm fabriqué à l’étranger, les Covidiens japonais patriotes vont enfin avoir la possibilité d’introduire dans leur circulation sanguine des nanoparticules lipidiques de fabrication nationale. D’après NHK World.
Un groupe d’experts du Ministère japonais de la santé a déclaré qu’un vaccin contre le coronavirus mis au point par Daiichi Sankyo pouvait être utilisé pour les inoculations au Japon. Il s’agirait du premier vaccin COVID fabriqué au Japon et utilisable dans la pratique.
Seriez-vous surpris d’apprendre que la majorité des membres du panel porte encore des masques?

Le groupe d’experts s’est réuni lundi. Les experts ont déclaré qu’ils confirmaient l’efficacité du vaccin et qu’ils n’avaient aucune inquiétude sérieuse quant à sa sécurité.
Banzaï! Malheureusement, l’article ne donne aucun détail sur l’efficacité que les experts ont apparemment confirmée. Heureusement, Daiichi-Sankyo avait déjà publié un communiqué de presse annonçant joyeusement que le critère principal avait été atteint dans l’essai de phase 3 de son vaccin Covid (DS-5670). Le DS-5670 a-t-il donc atteint une efficacité de 95%, comme ceux de Pfizer/BioNTech et de Moderna ?
Les principaux critères d’évaluation de l’essai de vaccination de rappel [boosters] étaient la moyenne géométrique du titre d’anticorps neutralisants dans le sang et la réponse immunitaire contre le SARS-CoV-2 (sous-variant omicron BA.5) quatre semaines après la vaccination expérimentale. Les résultats sur les critères d’évaluation dans le groupe DS-5670 étaient plus élevés que ceux du groupe témoin (vaccin bivalent adapté à l’omicron et approuvé au Japon), démontrant statistiquement la non-infériorité du DS-5670.
En d’autres termes, le DS-5670 a produit plus d’anticorps contre le BA.5 que le vaccin bivalent de Pfizer/BioNTech ou de Moderna, dont l’efficacité n’a jamais été démontrée. Combien de plus? On ne sait pas encore.
Les résultats détaillés de l’essai de vaccination de rappel seront présentés lors de conférences universitaires et dans des publications.
Vous vous dites peut-être: « Minute. Vous êtes en train de me dire que le Japon vient d’approuver une toute nouvelle injection de Covid basée sur des titres d’anticorps non publiés? » Ouaip, c’est exactement ce que je suis en train de vous dire.
Mais Daiichi-Sankyo utilise la même plate-forme d’ARNm que Pfizer/BNT et Moderna. Ce n’est donc pas comme si le Ministère de la Santé, du Travail et des Affaires Sociales (MSTAS) leur donnait le feu vert pour une nouvelle technologie.
L’ascension des réplicons
En revanche, le Ministère de la Santé, du Travail et des Affaires Sociales donne son feu vert à une nouvelle technologie pour Meiji Seika Pharma1. Extrait du communiqué de presse de l’entreprise.
Meiji Seika Pharma Co., Ltd. a annoncé aujourd’hui qu’elle avait reçu l’approbation pour la fabrication et la commercialisation de « Kostaive™ pour injection intramusculaire » (ARCT-154), un vaccin ARNm auto-amplifiant contre le COVID-19, de la part du Ministère de la Santé, du Travail et des Affaires Sociales (MSTAS) au Japon.
Il s’agit de la première approbation au monde d’un vaccin à ARNm auto-amplifié. Qu’est-ce qu’un vaccin à ARNm auto-amplifié? Un vaccin à ARNm qui s’auto-amplifie, évidemment.
L’ARNm contenu dans Kostaive est conçu pour s’auto-amplifier une fois délivré dans les cellules, de sorte qu’il génère une forte réponse immunitaire et offre la possibilité d’une protection de longue durée tout en utilisant des doses d’ARNm inférieures à celles des vaccins ARNm existants.
En d’autres termes, vos cellules peuvent devenir des usines à ARNm encore plus efficaces. L’image et la description ci-dessous sont tirées d’un article de la revue d’immunologie Cell, au titre inquiétant: « Rise of the RNA machines – self-amplification in mRNA vaccine design » (L’ascension des machines à ARN – l’auto-amplification dans la conception des vaccins à ARNm). Il convient de noter que l’ARNm auto-amplifié peut également être appelé ARN réplicon.
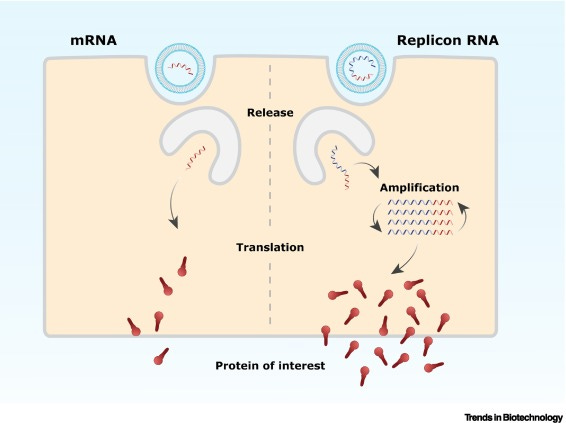
Une fois libéré dans la cellule, l’ARNm est traduit pour produire la protéine en question. Contrairement à l’ARNm, l’ARN réplicon code avec la protéine d’intérêt, des gènes d’auto-amplification (représentés en bleu) qui amplifient l’ARN réplicon. Cette amplification intracellulaire se traduira par la suite par des niveaux d’expression plus élevés de la protéine en question.
Je ne prétends pas être un expert en la matière, mais je doute que cela puisse résoudre le problème de la surproduction de protéines de pointe [NdT. ma traduction ici] observé avec la plateforme ARNm d’origine. C’est d’ailleurs ce que suggère l’article de Cell.
À l’heure actuelle, les principaux défis liés à l’autorisation mondiale sont les problèmes de sécurité potentiels concernant le caractère réplicatif de ces vaccins… Par exemple, les vaccins à réplicon pourraient persister chez les personnes immunodéprimées, car la clairance pourrait être moins efficace.
Étant donné qu’aucun autre vaccin à ARNm auto-amplifié n’a été approuvé auparavant, le MSTAS a au moins exigé que l’entreprise réalise un essai contrôlé randomisé à grande échelle pour tester l’efficacité réelle du vaccin contre les infections et les maladies graves, n’est-ce pas? Haha, non. Revenons au communiqué de presse.
Dans les essais cliniques de phase III pour la vaccination de rappel menés au Japon, 5 μg de Kostaive™ ont suscité des titres d’anticorps neutralisants plus élevés (p<0,05) et plus durables contre la souche originale, ainsi que le sous-variant Omicron BA 4-5, par rapport à 30 μg de COMIRNATY ®, un vaccin ARNm conventionnel homologué ciblant le COVID-19.
Au moins, cette fois-ci, une préimpression est disponible (ici). Alors que l’essai de phase 3 pour le Comirnaty de Pfizer/BNT a débuté avec environ 40 000 participants non vaccinés, celui-ci n’en comptait que 828, qui avaient tous reçu trois injections auparavant. Un essai à si petite échelle ne peut clairement pas nous dire si la nouvelle plateforme pose les mêmes problèmes de sécurité que la plateforme originale, et encore moins des problèmes différents (ce qui est en quelque sorte le but). Mais il est intéressant de noter que Kostaive (ARCT-154) a tout de même réussi à amplifier les taux de frissons, de maux de tête et de myalgies (douleurs musculaires) par rapport à Comirnaty, et ce malgré une posologie six fois moindre. C’est la magie de l’auto-amplification, je suppose.
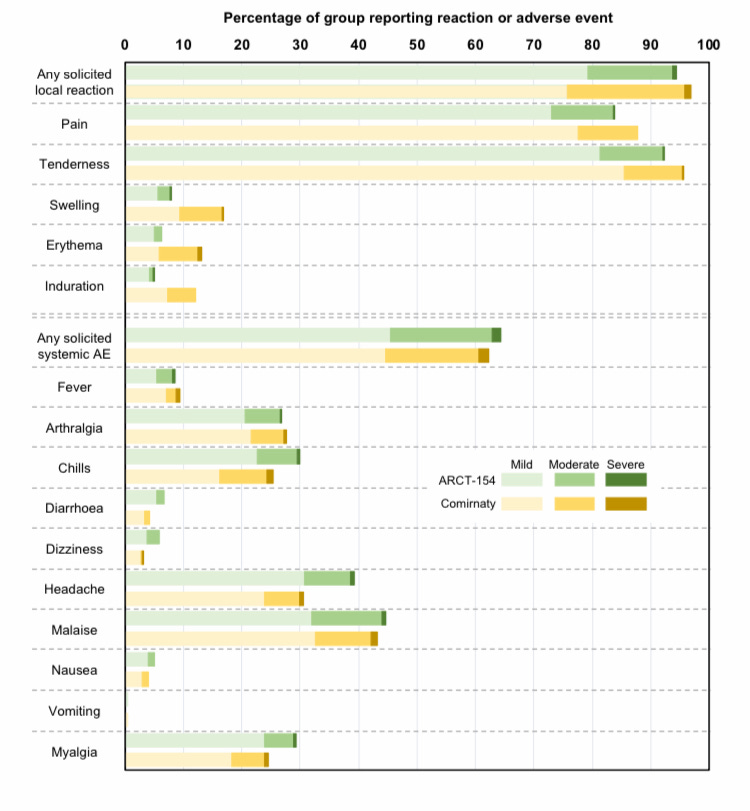
Cependant, la version de Kostaive utilisée dans l’essai ciblait le virus de type sauvage qui a disparu de la circulation au début de 2021, de sorte que Meiji Seika Pharma ne commercialisera pas cette version. Au lieu de cela, l’entreprise prévoit de commercialiser une version actualisée de Kostaive en 2024 et mène actuellement un autre essai de phase 3 sur une version bivalente, en comparant à nouveau les titres d’anticorps.
Ainsi, non seulement le MSTAS a approuvé un vaccin utilisant une nouvelle technologie sur la base des titres d’anticorps, mais il ne l’a même pas approuvé sur la base des titres d’anticorps du vaccin qui sera effectivement mis sur le marché. L’ancienne définition de « réglementation », comme celles de « sûr » et « efficace », semble être morte du Covid.
Il semble que ce soit l’un des héritages durables de la pandémie de Covid-19: les organismes de réglementation ont abandonné toute prétention à faire correctement leur travail et se contentent d’approuver sans broncher toute demande d’autorisation émanant d’entreprises favorisées sur la base de données essentiellement dénuées de sens. Malgré ce qu’ils prétendent, les experts du MSTAS n’ont pas confirmé que les nouveaux vaccins offraient un quelconque avantage à qui que ce soit d’autre que les fabricants de vaccins, mais ils ont confirmé qu’eux-mêmes n’en offraient certainement pas.
- Comme Pfizer, Meiji Seika Pharma fabriquera son injection sous licence: « Meiji Seika Pharma a obtenu de CSL Seqirus les droits exclusifs de distribution de Kostaive™ (ARCT-154) au Japon le 11 avril 2023. » ↩︎